Бактерии изменяют свои рибосомы под воздействием широко распространенных антибиотиков, говорится в исследовании Центра геномной регуляции в Барселоне, опубликованном в журнале Nature Communications. Этих тонких преобразований, которые представляют собой возможный новый механизм устойчивости к антибиотикам, может быть достаточно, чтобы изменить место связывания лекарственных мишеней.
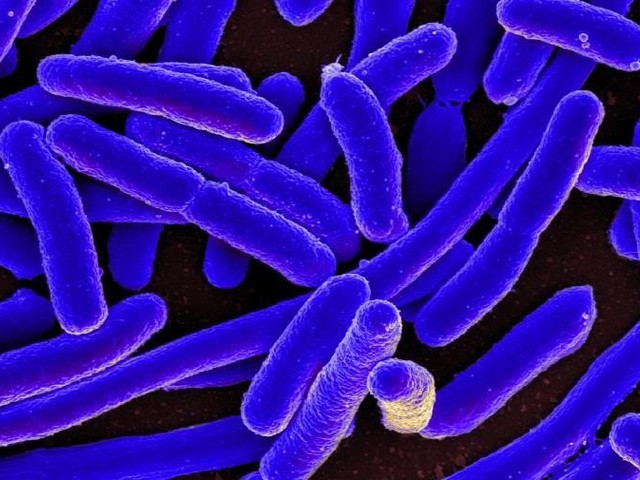
Кишечная палочка – распространенная бактерия, которая часто бывает безвредной, но иногда может вызывать серьезные инфекции. Исследователи подвергли кишечную палочку воздействию стрептомицина и касугамицина – двух препаратов, которыми лечат бактериальные инфекции. Стрептомицин используется против туберкулеза и других инфекций с 1940-х годов, а касугамицин менее известен, но крайне важен в сельском хозяйстве для предотвращения бактериальных заболеваний сельскохозяйственных культур.
Оба антибиотика нарушают способность бактерий создавать новые белки, целенаправленно воздействуя на их рибосомы. Эти молекулярные структуры создают белки и сами состоят из белков и рибосомальной РНК. Последняя часто модифицируется химическими метками, которые могут изменять форму и функции рибосомы. Клетки используют метки для тонкой настройки производства белков.
Исследование показало, что в ответ на антибиотики кишечная палочка начинает собирать новые рибосомы, которые немного отличаются от тех, что производятся в обычных условиях. В зависимости от того, какой антибиотик использовался, новые рибосомы не имели определенных меток, они были потеряны именно в тех областях, где антибиотики цепляются и останавливают производство белка. Это делает бактерии более устойчивыми к лекарствам.
«Мы думаем, что рибосомы бактерий могут изменять свою структуру настолько, чтобы антибиотик не мог эффективно связываться с ними», – говорит Анна Дельгадо-Техедор, первый автор исследования. Известно, что бактерии развивают устойчивость к антибиотикам разными способами, включая мутации в их ДНК. Другим распространенным механизмом является их способность активно выкачивать и транспортировать антибиотики из клетки, снижая концентрацию лекарства внутри клетки до уровня, который не является вредным.
Данное исследование свидетельствует о совершенно новой стратегии выживания. «Кишечная палочка изменяет свои молекулярные структуры с поразительной точностью в режиме реального времени. Это скрытный и тонкий способ уклонения от лекарств», – говорит доктор Ева Новоа, автор-корреспондент исследования.
Исследователи сделали выводы, используя передовую технологию нанопорового секвенирования, которая считывает молекулы РНК напрямую. Предыдущие методы обрабатывали молекулы РНК таким образом, чтобы удалить химические модификации. «Наш подход позволил увидеть модификации такими, какие они есть, в их естественном контексте», – говорит доктор Новоа.
Дальнейшие исследования позволят изучить биологию, лежащую в основе этого адаптивного механизма, и открыть новые способы борьбы с одним из самых серьезных кризисов в мировом здравоохранении. С 1990 года глобальная устойчивость к противомикробным препаратам ежегодно уносит по меньшей мере миллион жизней, а в период до 2050 года, по прогнозам, унесет еще 39 миллионов жизней.
«Если мы проникнем глубже и поймем, почему бактерии производят эти модификации, мы сможем разработать новые стратегии, которые не позволят бактериям делать этого, или создать лекарства, которые будут более эффективно связываться с измененными рибосомами», – говорит доктор Новоа.
Автор: Анна Щербакова
Заглавное фото: NIAID / Anna Delgado-Tejedor